
Marek Toráč | 25.3.2025
Uplatnění zaplacených úroků z úvěru bytových družstev v daňovém přiznáníDaně, účetnictví, právo a nejen to. Všechny klíčové novinky pro váš byznys.
Jiří Jakoubek | Blanka Trefná | 9. Března 2023
Rádi bychom vás informovali o možných implikacích Cenového předpisu Ministerstva zdravotnictví[1], který nabyl účinnosti na počátku letošního roku, a to s ohledem do jeho dopady do oblasti převodních cen.
Hlavním cílem cenového předpisu je úprava regulace ceny léčivých přípravků nebo potravin určených pro zvláštní lékařské účely, jsou-li hrazeny z veřejného zdravotního pojištění, a to bez ohledu na to, zda jsou v daném konkrétním případě skutečné hrazeny z prostředků veřejného zdravotního pojištění nebo zda si je plně hradí pacient. Cenová regulace je zabezpečena dvojím způsobem, tj. regulací ceny původce stanovením maximální ceny a regulací obchodní přirážky[2] stanovením maximální obchodní přirážky.
Z hlediska dopadu do problematiky převodních cen je zásadní změna v úpravě definice pojmů jiná osoba a cena původce.
|
úprava účinná do 31. 12. 2022 |
Nová úprava účinná od 1. 1. 2023 |
|
„jinou osobou uvádějící registrovaný přípravek na trh (se rozumí) – osoba oprávněná k distribuční činnosti, která uvádí registrované hromadně vyráběné léčivé přípravky na trh v České republice, přičemž není v postavení držitele rozhodnutí o jejich registraci a ani je nedodává jejich držiteli rozhodnutí o registraci.“
|
„jinou osobou dodávající léčivý přípravek na trh (se rozumí) - osoba oprávněná k distribuční činnosti, která dodává hromadně vyráběné léčivé přípravky na trh v České republice a s původcem tvoří koncern nebo byla původcem jako jediná písemně pověřena k dodávání takových přípravků na trh v České republice.“ |
Prvotní úpravou se mění samotné určení jiné osoby a to na osobu dodávající léčivý přípravek na trh - nikoliv pouze uvádějící registrovaný přípravek na trh, jak tomu bylo v dosavadní úpravě. Jiná osoba je tedy definována případy, kdy se jedná o:
Nově je tedy Cenovým předpisem zaveden ve vztahu k jiné osobě dodávající léčivý přípravek na trh požadavek, aby tato jiná osoba byla součástí koncernu s původcem, případně byla původcem exkluzivně a písemně pověřena.
Menší změna proběhla i v případě definice pojmu cena původce. V novém znění se jedná o cenu, za kterou je léčivý přípravek dodáván původcem nebo jinou osobou dodávající daný přípravek na trh v ČR další osobě (nahradila původní znění: cena, za kterou dodá první osobě) oprávněné léčivý přípravek distribuovat nebo vydávat, bez obchodní přirážky a DPH.
Nový cenový předpis zavádí definici pro pojem cena pro konečného spotřebitele, která je vymezena jako součet skutečně uplatněné ceny původce, obchodní přirážky a DPH.
Výše uvedené změny shrnuje následující zjednodušené schéma.
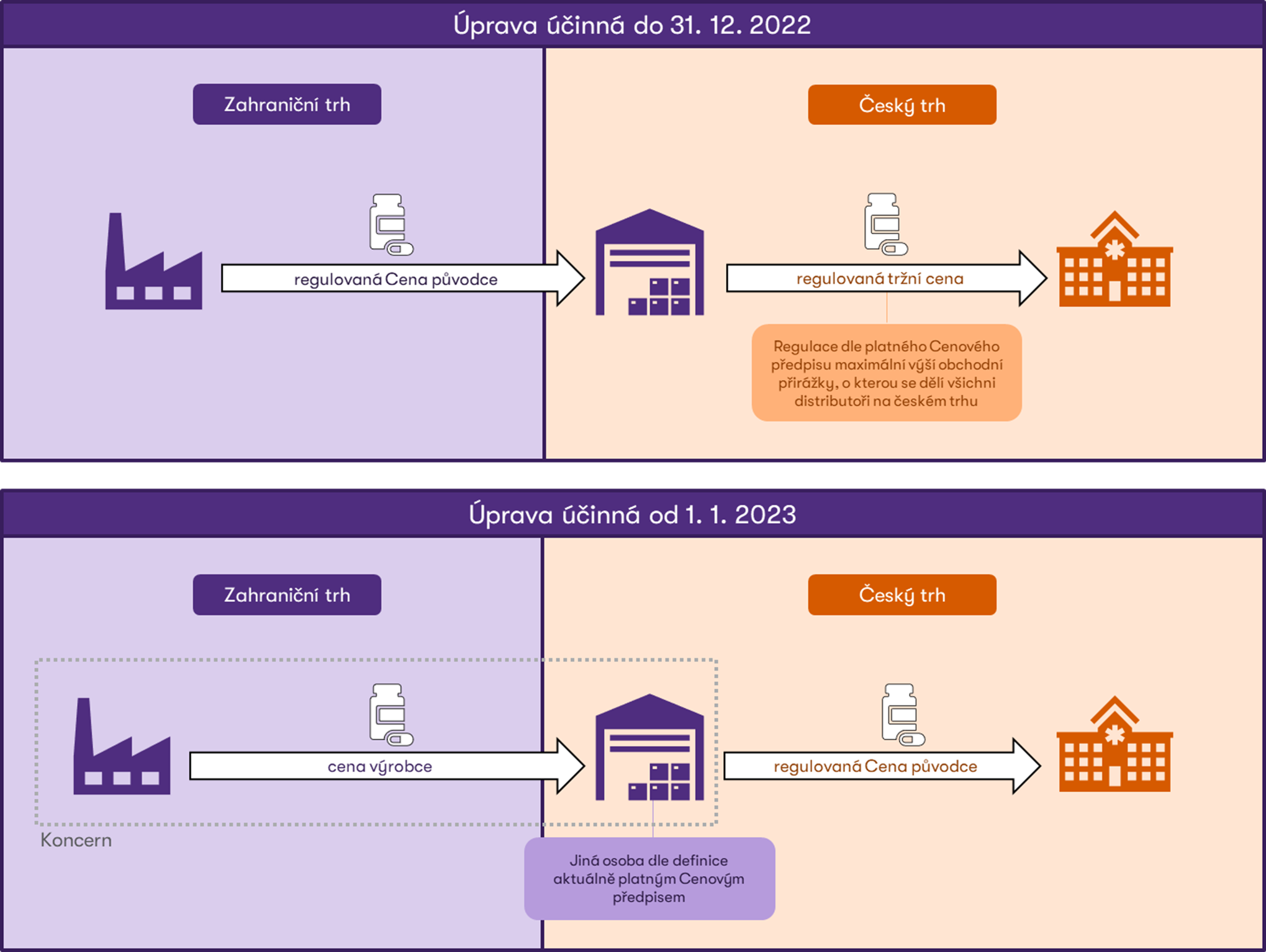
V souvislosti s výše uvedenou změnou vyvstává řada otázek nejen v souvislosti s problematikou převodních cen.
Nový cenový předpis může ovlivnit stávající způsob cenotvorby mezi původcem a distributorem, který splňuje podmínky stanovené aktuálně platným Cenovým předpisem pro definici jiné osoby, neboť v tomto případě cena, za kterou léčivý přípravek vstupuje na český trh je regulována tzv. cenou původce na úrovni jiné osoby a současně by měla splňovat daňová pravidla vztahující se k oblasti převodních cen.
V případě, že se výše uvedené dopady Cenového předpisu dotýkají vnitroskupinových transakcí realizovaných vaší společností, velmi rádi vám budeme asistovat při revizi stávajícího modelu cenotvorby s ohledem dodržení principu tržního odstupu při současném respektování pravidel, která ukládá aktuálně platný Cenový předpis.
[1] Jedná se o cenový předpis Ministerstva zdravotnictví č. 2/2023OLZP, o regulaci cen léčivých přípravků a potravin pro zvláštní lékařské účely, který nahrazuje stávající Cenový předpis Ministerstva zahraničí č. 1/2020/CAU ze dne 10. prosince 2019 o regulaci cen léčivých přípravků a potravin pro zvláštní lékařské účely, který byl v platnosti od ledna 2020.
[2] U léčivých přípravků a potravin pro zvláštní účely, stanovených odst. 7 článku II. Cenového předpisu (např. hromadně vyráběná registrovaná radiofarmaka) podléhá regulaci pouze obchodní přirážka.
[3] Původcem se u léčivých přípravků zpravidla rozumí držitel rozhodnutí o registraci, je-li léčivý přípravek registrován, nebo dovozce případně tuzemský výrobce.